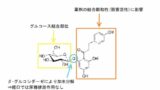
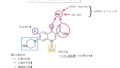
DPP–4阻害薬 の化学構造とファーマコフォアを解説します。
DPPー4阻害薬は化学構造と結合様式から3つのクラスに分けられ、近年は薬剤師国家試験にも化学構造やファーマコフォアの問題も出題されているので薬学生の方もチェックしておきましょう。
DPP–4阻害薬のクラス分けについては以下2冊の書籍でも言及されていますが、
化学構造式とファーマコフォアの解説は【臨床医薬品化学】の方が詳しくおすすめです!
『医薬品構造化学』も化学構造式の勉強にはよくまとまっている良書です。
そのほか、おすすめの書籍は「【化学構造式の勉強におすすめの本・書籍】構造式と薬理作用の関係を臨床へ活かせる本を紹介!」で紹介しているので、興味のある方は参考にしてください。
DPP・インクレチン と DPP–4阻害薬
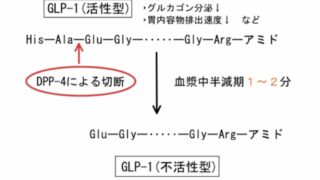
「DPP」は”ジペプチジルペプチダーゼ”の略で、文字通りアミノ酸2個分(ジペプチド)でタンパク質を分解する働きを持ち、インスリン分泌作用のあるインクレチン(GLP-1、GIP)を不活性化します。
DPP-4は腸・肝・腎、血管内皮などに多く発現しており、DPP-4阻害薬はインクレチンの分解を抑制し、インスリン分泌能を高い状態に保ち血糖を下げることができます。本来インクレチンは半減期がせいぜい1〜2分という短さで消失していきます。
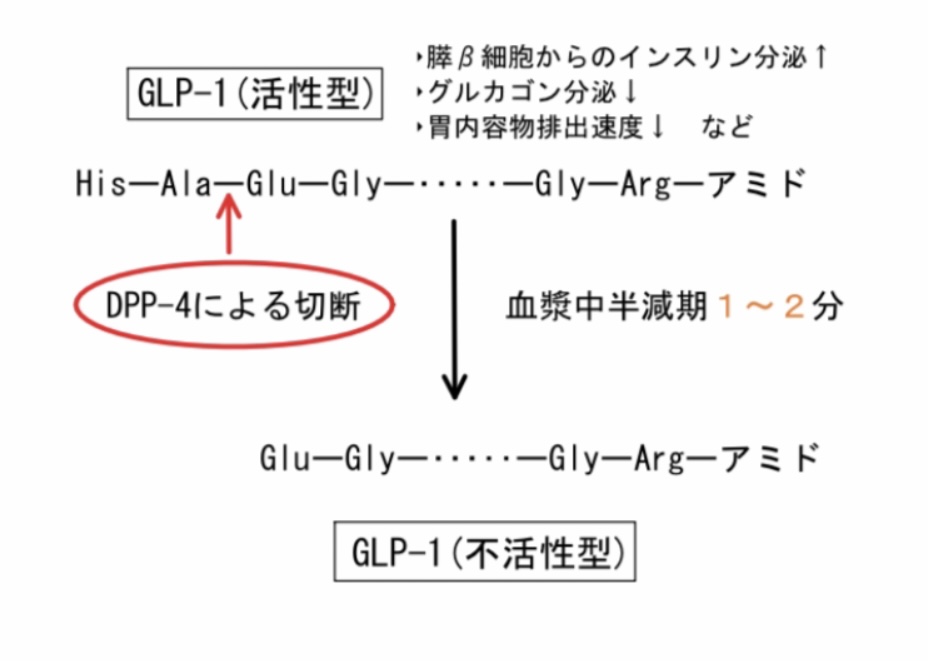
また、DPPにはサブタイプとしてDPP-8やDPP-9などがあり、解明はされていないものの、これらを阻害してしまうと毒性に関与するとされ、DPP-4への選択性も重要となっているようです。
第106回薬剤師国家試験 問210–211
第106回薬剤師国家試験でもDPP–4阻害薬のファーマコフォアに関する問題が出ています。
ファーマコフォアの知識がなくても解ける問題ですが、薬理作用の本質が相互作用であることを学ぶ意味で良問だと思います。

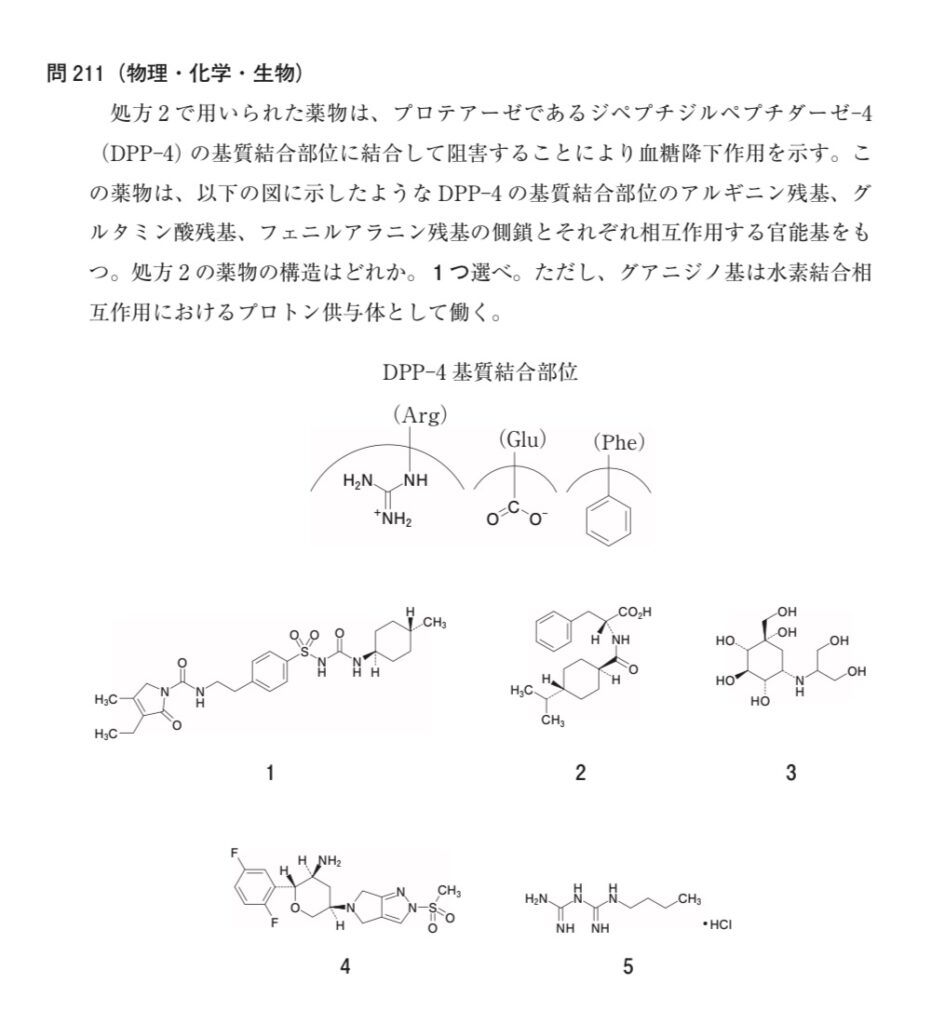
正答. 問210→2、問211→4
問211に関して少し解法のポイントを加えると、
- 問題文最後に「グアニジノ基は水素結合相互作用におけるプロトン供与体として働く」とあり、水素結合可能な原子・置換基を持つと予想
- Glu残基のカルボキシ基は塩基性アミンと静電相互作用(イオン結合)すると予想
- Phe残基はファンデルワールス相互作用(π–π相互作用)すると予想
これらを全て満たす4の化学構造式(オマリグリプチン)を選択することになります。
※本記事では水素結合も静電相互作用として表記しています。
DPP–4阻害薬 と クラス
DPP-4阻害薬は、その化学構造やDPP-4との結合様式などから主に3クラスに分けることができます。
(開発のきっかけとなった化合物や経緯でクラス分けされる場合もありますが、受容体結合の本質は結合様式のため化学構造と結合様式で分けていきます)
DPP-4中の結合部位のうち「S2拡張サイト」や「S1’、S2’サイト」と呼ばれるサイトでは、通常のS1、S2サイトよりも、より強力にDPP-4を阻害できる可能性もあるようです。
DPP-4阻害薬の全てに共通するのは、アミノ基がDPP-4のGlu205、Glu206との静電的相互作用を引き起こしDPP-4を阻害するために必須の相互作用をしていることです。
クラスⅠ
ビルダグリプチン、サキサグリプチン
クラスⅠは非常に構造がよく似ていて阻害活性はサキサグリプチン(オングリザ®︎)がビルダグリプチン(エクア®︎)より強く、サキサグリプチンに含まれるシクロプロパンが近傍の受容体アミノ酸と疎水性相互作用によって安定化しているためとされ、ちょうどS1部位の疎水ポケットに入り込む位置にあります。
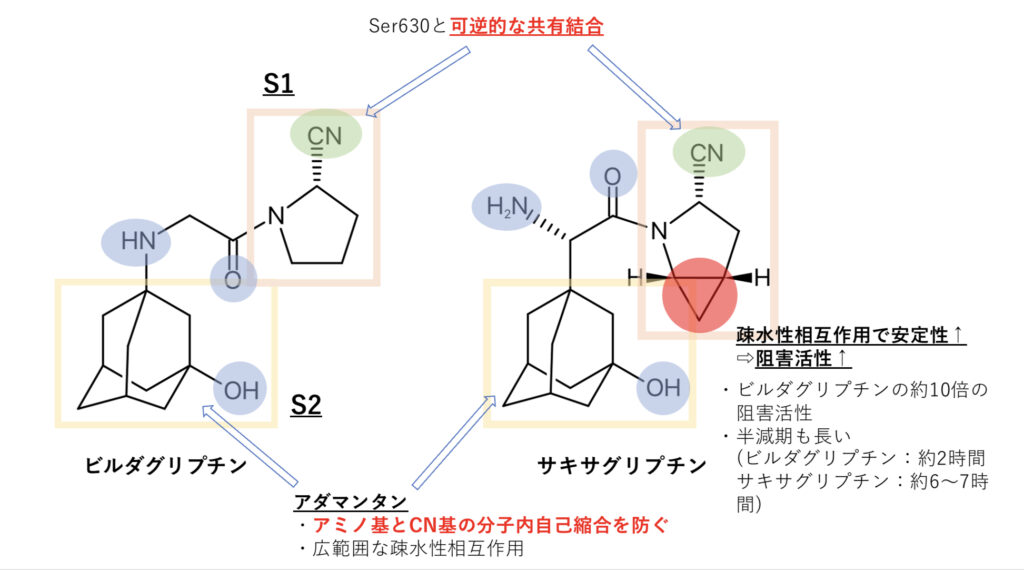
共通している大きな特徴は2つ
①シアノ基(–C≡N)がDPP–4と可逆的な共有結合を形成
②アミノ基とシアノ基の自己縮合を防ぐため嵩高いアダマンチル基を導入
立体的に嵩高いアダマンタン骨格がアミノ基とシアノ基の分子内反応を防いでいると考えられています。
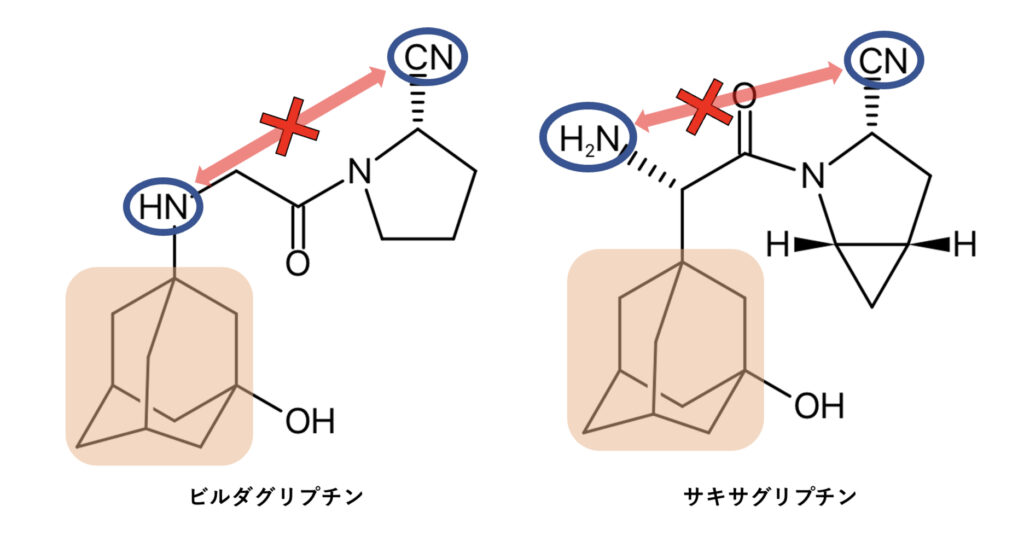
クラスⅡ
アログリプチン、トレラグリプチン
クラスⅡで特徴的なのはアログリプチン(ネシーナ®︎)とトレラグリプチン(ザファテック®︎)です。
見ての通り、トレラグリプチンはアログリプチンにたった1個のF原子が導入された化学構造になっています。
たったこれだけの違いで薬剤プロファイルが大幅に変化するのは、さすが偉大なF原子です!
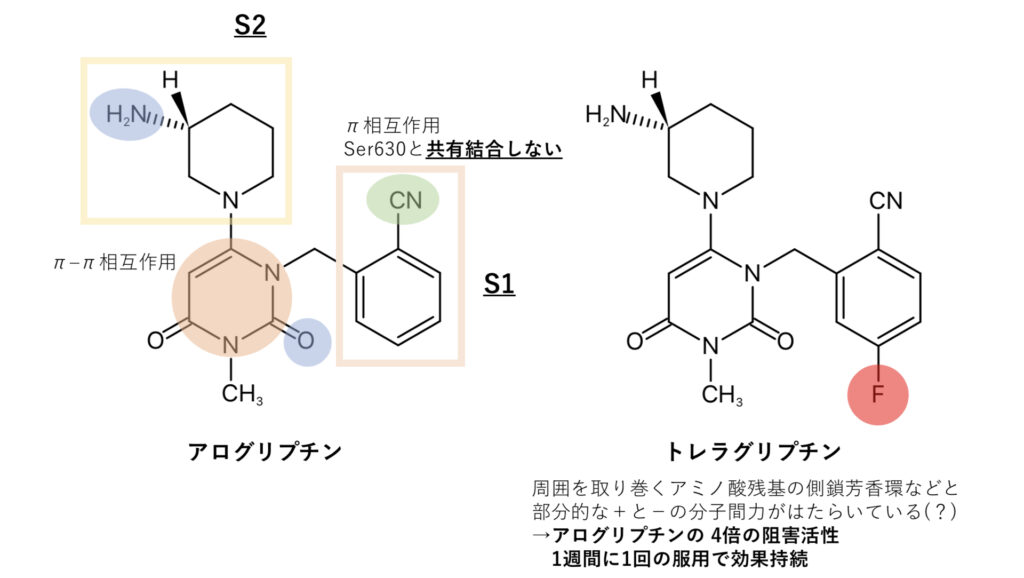
周囲のアミノ酸残基の側鎖芳香環などと部分的な静電相互作用に近い分子間力によって、アログリプチンよりも優れた阻害活性や持続性を獲得しています。
トレラグリプチンはアログリプチンの4倍の阻害活性を持ち、服用回数も1週間に1回と持続性が非常に高いこともわかります。
リナグリプチン
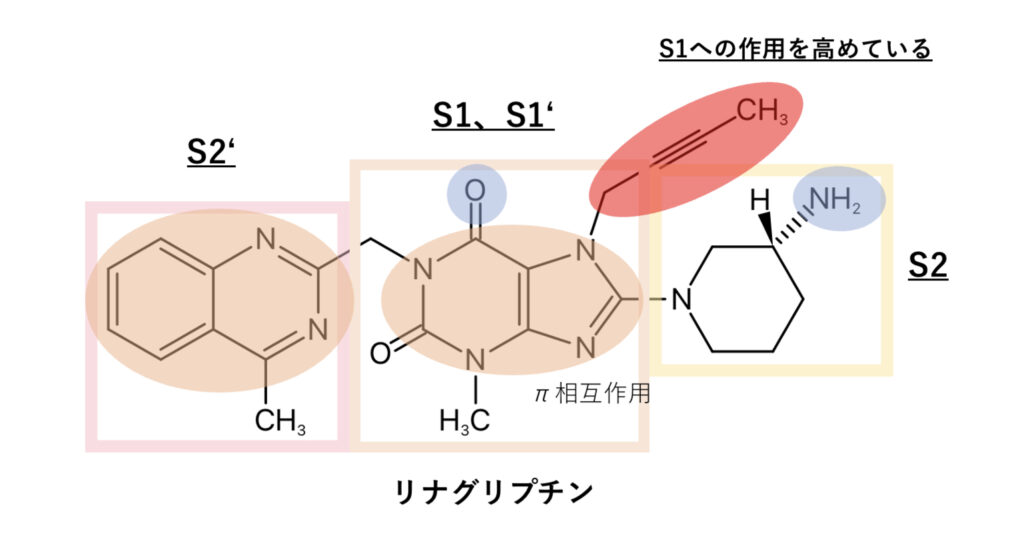
クラスⅢ
クラスⅢでは、構造式の端にある芳香環含む2個の環構造が「S2拡張サイト」に結合し、DPP-4との親和性が高められています。
アナグリプチン
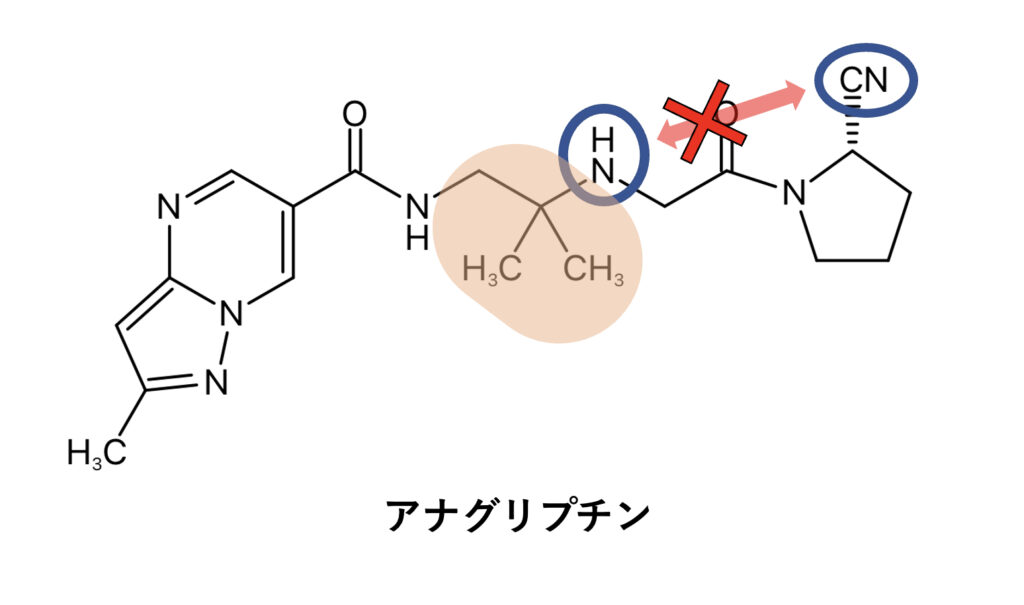
アナグリプチンはCN基を持つもののSer630のOH基とは共有結合しないとされていますが、X線解析の結果から受容体と相互作用する際の中間体の段階では共有結合している可能性があるようです。
また、阻害活性がシタグリプチンやアログリプチンよりも弱いのは、CN基が受容体と共有結合を形成することでS1部位での疎水性相互作用が遅れているためとも考えられています。
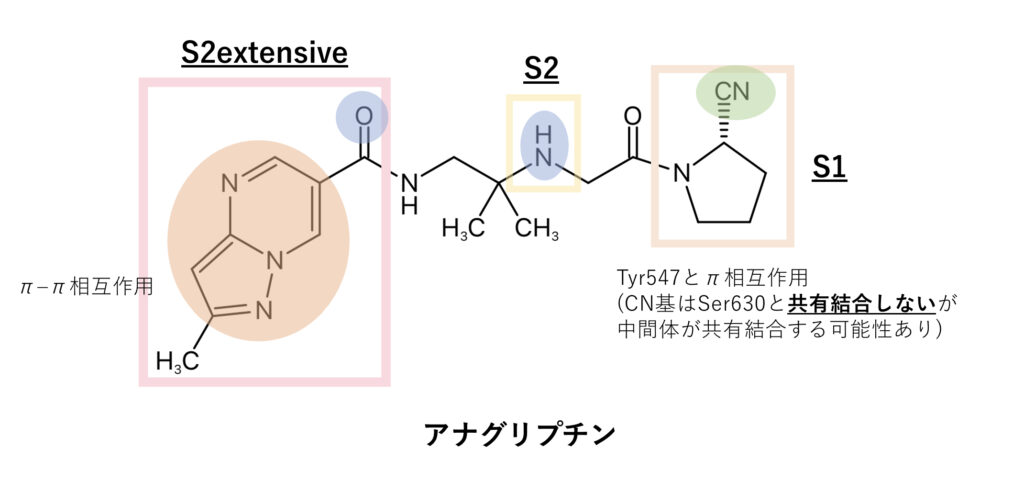
さらに構造式中の3級炭素(下図の橙色部分)はクラスⅠのビルダグリプチンやサキサグリプチンのように、分子内でアミノ基とシアノ基が反応しないように嵩高い置換基の役割を果たしているとされています。
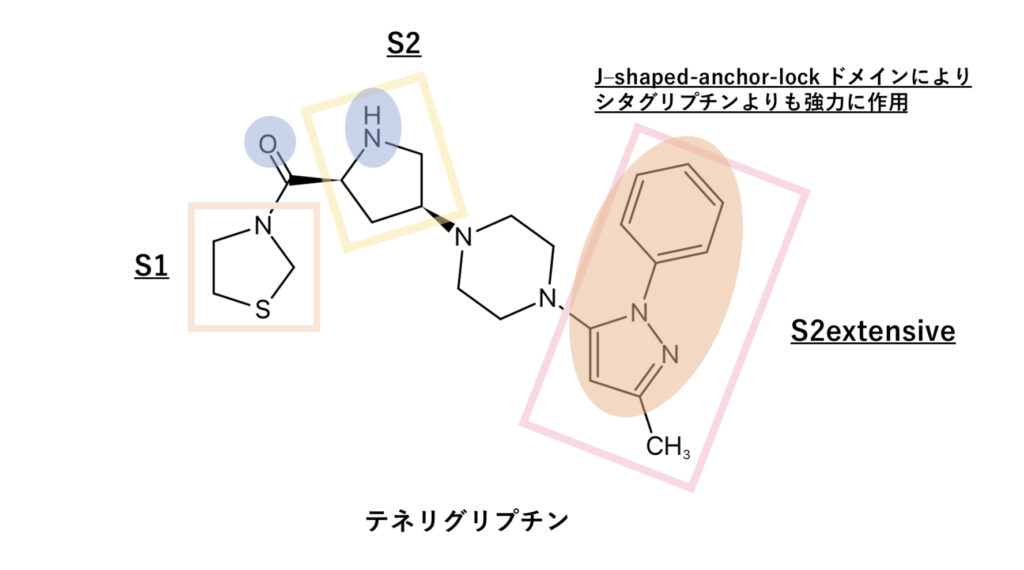
テネリグリプチン
テネリグリプチンはS2extensive部位で「J」の形をした釣り針の“返し“のような大きな置換基によって受容体にフィットし、シタグリプチンよりも強力に作用しているようです。
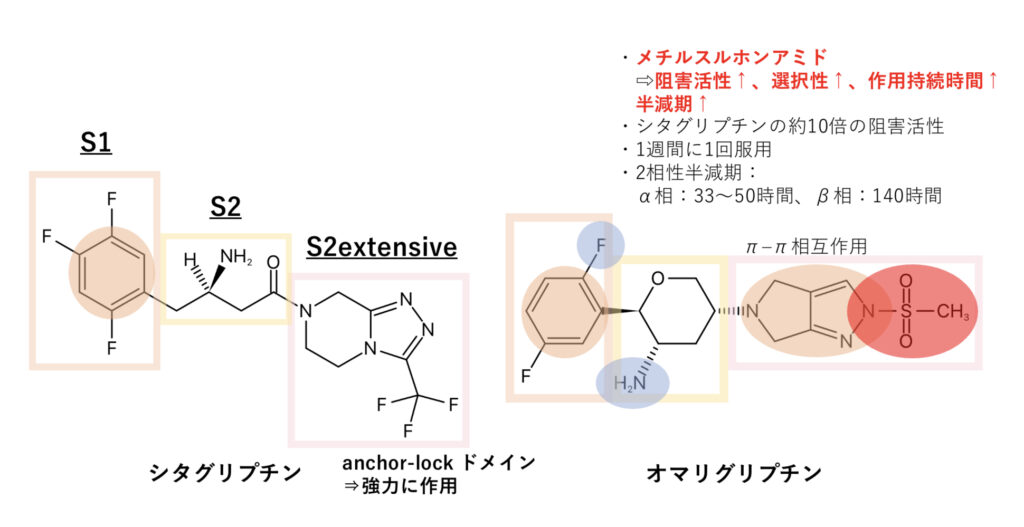
シタグリプチン、オマリグリプチン
シタグリプチンもS2extensive部位でテネリグリプチンのような“返し“で受容体に固定されています。
オマリグリプチンの構造活性相関を見ると、S1部位とS2extensive部位に作用する構造がtransの位置にあることがDPP–4を阻害するのに必須で、スルホンアミド構造によって阻害活性、DPP–4選択性、作用時間(半減期)が向上しているのが特徴です。
スルホンアミドは薬剤の水溶性や代謝安定性を向上させるため、他の薬剤でもよく見られる重要な置換基の一つです。
DPP–4阻害薬 の強さ比較
例によって強さを“大まかに”比較してみます。
阻害活性は、
シタグリプチン<アログリプチン<アナグリプチン≒リナグリプチン≒ビルダグリプチン<テネリグリプチン<オマリグリプチン≦トレラグリプチン<サキサグリプチン
通常用量に換算すると、
リナグリプチン(5)<シタグリプチン(50)≦アログリプチン(25)<テネリグリプチン(20)≦オマリグリプチン(25)≦ビルダグリプチン(50)≒サキサグリプチン(5)<トレラグリプチン(100)
と、だいたいこのような順になりました。
直接比較のデータは無さそうで、用法も考慮していないので参考程度です。
DPP-4阻害薬は効果自体がそれほど強力ではないものの、HbA1cを下げつつ食後高血糖も同時に防ぎたい場合に有用です。DPP-4阻害薬には多くの種類がありますが、効き目が得られない場合には、結合様式の異なるクラスに替えることでHbA1cを下げることができる可能性がある(※)という報告もあります。
効果不十分で同種同効薬に切り替える場合、無闇な切り替えをするくらいならクラススイッチを検討した方が良いかもしれません。
患者さんのアドヒアランスや生理的条件も考慮しながら選択できればと思います。
あわせて読みたい記事
参考:
- Joel P Berger et al. A comparative study of the binding properties, dipeptidyl peptidase-4 (DPP-4) inhibitory activity and glucose-lowering efficacy of the DPP-4 inhibitors alogliptin, linagliptin, saxagliptin, sitagliptin and vildagliptin in mice. Endocrinol Diabetes Metab. 2017.
- Charles E Grimshaw et al. Trelagliptin (SYR-472, Zafatek), Novel Once-Weekly Treatment for Type 2 Diabetes, Inhibits Dipeptidyl Peptidase-4 (DPP-4) via a Non-Covalent Mechanism. PLoS One. 2016.
- Mika Nabeno et al. A comparative study of the binding modes of recently launched dipeptidyl peptidase IV inhibitors in the active site. Biochemical and Biophysical Research Communications. 434, 2, 3 May 2013, 191-196
- Yukihisa S Watanabe et al. Anagliptin, a potent dipeptidyl peptidase IV inhibitor: its single-crystal structure and enzyme interactions. J Enzyme Inhib Med Chem. 06 Jul 2015
- Katsuhiko Mizuno et al. Identification of a novel metabolite of vildagliptin in humans: Cysteine targets the nitrile moiety to form a thiazoline ring. Biochem Pharmacol. 2018 Oct.
- William J Metzler et al. Involvement of DPP-IV catalytic residues in enzyme-saxagliptin complex formation. Protein Sci. 2008 Feb.
- Tesfaye Biftu et al. Omarigliptin (MK-3102): A Novel Long-Acting DPP-4 Inhibitor for Once-Weekly Treatment of Type 2 Diabetes. J. Med. Chem. 2014, 57, 8, 3205–3212. March 24, 2014
- (※)Yuta Suzuki et al. Clinical effectiveness of switching between DPP-4 inhibitors in patients with type 2 diabetes mellitus. Int J Clin Pharmacol Ther. 2019 Sep.
- Vishal Mathur, et al. Insight into Structure Activity Relationship of DPP-4 Inhibitors for Development of Antidiabetic Agents. Molecule 3;28(15):5860. 2023 Aug.
- DPP-4阻害薬 各種インタビューフォーム(IF)